
Molalitas atau molal YouTube
Menyadur dari laman Kompas.com, molalitas dapat diterapkan untuk menentukan titik didih, titik leleh, juga dapat dimanfaatkan ketika bekerja dengan sifat koligatif larutan, seperti kenaikan titik didih dan penurunan titik beku. Nah, bicara tentang molalitas itu sendiri terdapat rumusnya.

apa perbedaan molalitas dan molaritas Brainly.co.id
Molalitas - Pengertian, Rumus, dan Contoh Soal. Molalitas suatu larutan bisa diuji dengan menambahkan beberapa zat pelarut. Pada waktu membuat sirup, kamu tentu melarutkan sirup ke dalam air, semakin banyak sirup yang dilarutkan semakin manis minuman yang terjadi. Sirup disebut zat terlarut (solute) dan air disebut zat pelarut (solvent).

Rumus Perhitungan Molalitas dan Contoh Soal Jawab Rumus Kimia
Selain itu, jika istilah molaritas dinyatakan dengan huruf M besar, maka istilah untuk molalitas adalah huruf m kecil. 2. Rumus. Perbedaan molaritas dan molalitas juga terlihat pada rumus yang digunakan. Adapun rumus mencari molaritas adalah: Keterangan: M = Molaritas (M) n = Banyaknya mol zat terlarut (mol) V = volume larutan (L)

(DOC) Molaritas Molalitas Normalitas Rizal Faiz Academia.edu
Siswa perlu memahami apa itu molaritas dan apa itu molalitas agar dapat menggunakan rumus dengan tepat. Tidak sedikit siswa yang kebingungan untuk membedakan soal yang harus digunakan menggunakan rumus molaritas atau rumus molalitas. Untuk itu, tanyakan pada guru Anda jika ada beberapa penjelasan yang mungkin kurang Anda pahami.

Pengertian Molaritas dan Molalitas Larutan Lengkap Contoh Soal Kimia SMA Pakai Rumus Perhitungan
Molalitas, dilambangkan dengan huruf kecil m, adalah istilah yang digunakan untuk menggambarkan konsentrasi larutan. Molalitas dapat didefinisikan sebagai jumlah mol zat terlarut yang dilarutkan dalam 1 kilogram pelarut. Molalitas sama dengan mol zat terlarut (zat yang larut) dibagi dengan kilogram pelarut (zat yang digunakan untuk larut).
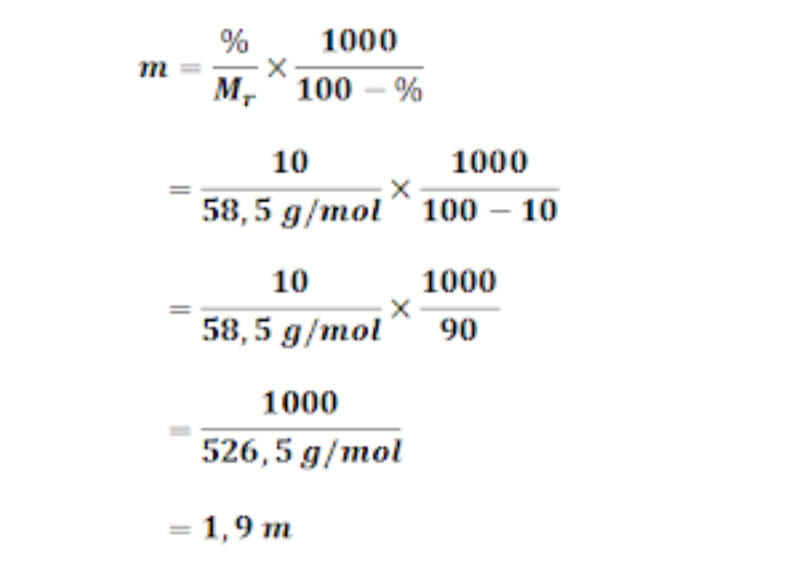
Cara Menghitung dan Contoh Soal Fraksi Mol dan Jawabannya Rumus dan Pembahasan Fraksi Mol
Zat yang dilarutkan ini menentukan sifat-sifat larutan tersebut yang dinamakan sebagai sifat koligatif larutan. Untuk mempelajari tentang sifat koligatif larutan, terlebih dulu kita harus mengetahui bagaimana cara menghitung konsentrasi larutan. Konsentrasi larutan adalah jumlah zat terlarut didalam larutan dalam satuan molaritas dan molaritas.

MOLARITAS DAN MOLALITAS CHEMISTRY EDUCATION YouTube
Apa Itu Konsentrasi Larutan? Sebelum membahas lebih dalam mengenai pengertian konsentrasi larutan, pastinya elo juga harus paham tentang larutan itu sendiri. Jadi, sebenarnya apa itu larutan?. Molalitas adalah satuan yang menyatakan jumlah mol suatu zat dalam satu kilogram larutan. Nah, bisa dilihatkan perbedaannya, jika molaritas.

Molalitas Larutan Nacl 10 Massa Dalam Air Adalah Mas Dayat Riset
Video ini berisi penjelasan dan contoh-contoh soal konsentrasi larutan yang meliputi molaritas, molalitas dan fraksi molOpen private class/kelompok belajar k.

MOLALITAS DAN FRAKSI MOLPEMBAHASAN SOAL (KELAS 12) 2 YouTube
Pengertian Molalitas. Molalitas adalah jumlah mol zat terlarut tiap 100 gram pelarut murni. Nilai molalitas dapat dihitung jika mol zat dan massa pelarut diketahui. Rumus Molalitas. Molalitas larutan dinyatakan dengan persamaan dibawah ini: molal = n/p. Dengan. n = jumlah mol zat pelarut (mol) p = massa pelarut (kg) molal = molalitas (mol/kg)

Apa perbedaan antara molaritas dengan molalitas
Molalitas ( m ) yaitu suatu satuan konsentrasi yang dapat menyatakan jumlah mol pada zat yang terdapat pada 1 kg pelarut dengan satuan mol. Demikianlah penjelasan terlengkap mengenai √ Molaritas, Molalitas, Normalitas, Fraksi Mol : Pengertian, Rumus & Contoh Soalnya Lengkap. Semoga bermanfaat dan bisa menambah ilmu pengetahuan bagi para.

Contoh Soal Molaritas Dan Pembahasannya
Baca juga: Soal UAS Kimia: Prinsip Molalitas dan Molaritas. Selain rumus molaritas, ada juga yang disebut sebagai persamaan molaritas. Dilansir dari GeeksforGeeks,. Apa Sajakah Itu? Skola. 06/03/2024, 08:00 WIB. 30 Contoh Kalimat Majas Personifikasi. Skola. 06/03/2024, 07:00 WIB. 10 Elemen-elemen Musik beserta Penjelasannya. Skola.
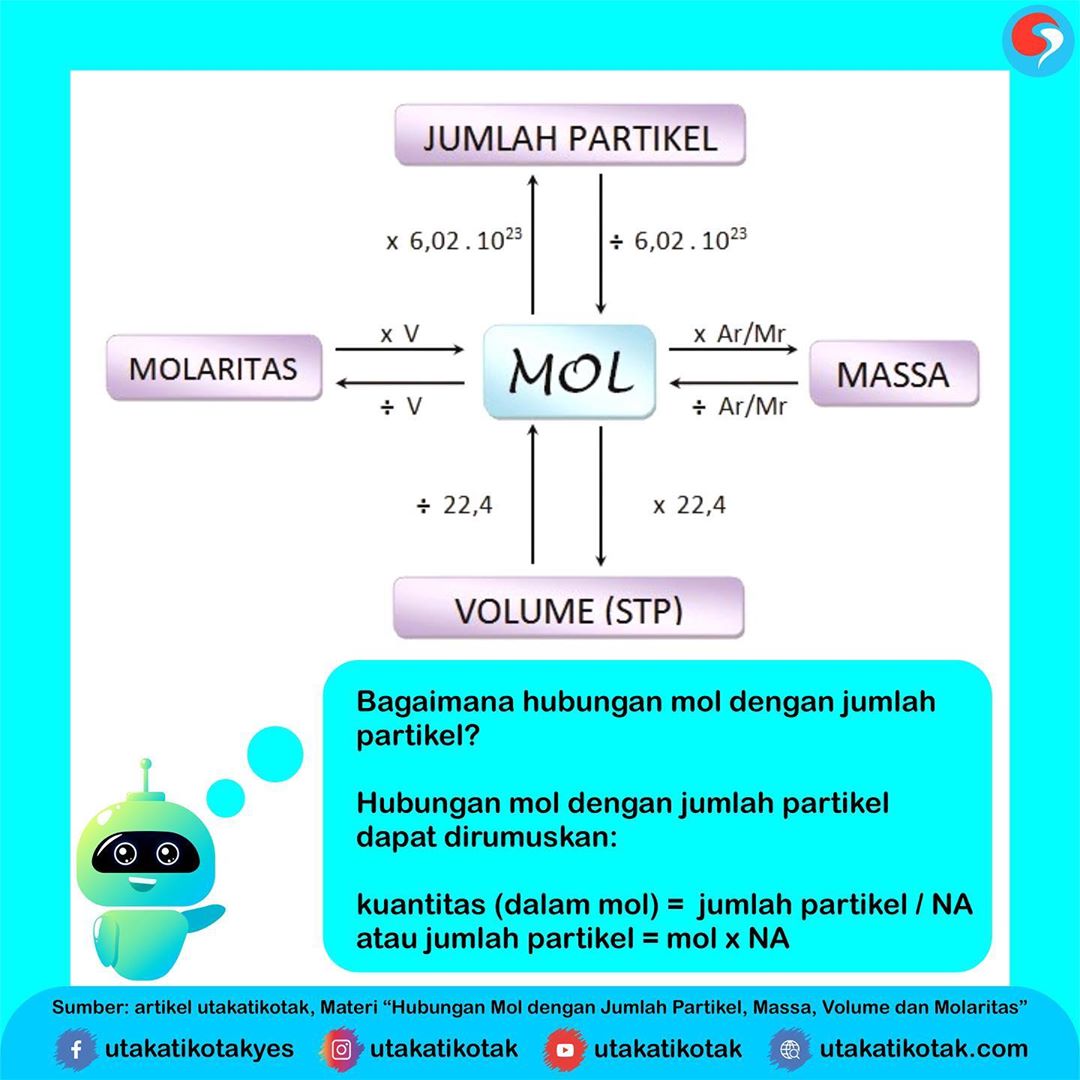
Hubungan Mol dengan Jumlah Partikel, Massa, Volume dan Molaritas
Chris Ryan / Getty Images. Molaritas dan molalitas keduanya merupakan ukuran konsentrasi larutan kimia. Molaritas adalah perbandingan mol dengan volume larutan (mol/L) sedangkan molalitas adalah perbandingan mol dengan massa pelarut (mol/kg). Sebagian besar waktu, tidak masalah unit konsentrasi mana yang Anda gunakan.

Fraksi Mol Dan Molalitas M Soal Dan Pembahasan Kimia Kelas 12 Riset
Contoh soal molalitas suatu larutan 20% berat C2H5OH (Mr = 46 g/mol) adalah.. Cara mengerjakan molalitas: C2H5OH 20% artinya 20 gram. C2H5OH dalam 80 gram air. m = massa x 1.000 = 20 x 1.000 = 5,4. Mr P 46 80. Jadi, kemolalan larutan 20% berat C2H5OH adalah 5,4 m. Selamat belajar contoh soal molalitas, detikers!

Rumus Molalitas dan Contoh Soal dan Pembahasannya!
Rumus Molalitas. Lalu, rumus molalitas itu apa ya, guys? Ini dia rumusnya: m = n/p. Keterangan: m : molalitas suatu zat (molal) n: mol suatu zat (mol) p: massa pelarut (g) Biar lebih paham cara mencari molalitas menggunakan rumus di atas, di bawah ini gue kasih latihan soal buat elo berlatih.

Rumus Molaritas dan Molalitas
Kapan Menggunakan Molaritas dan Normalitas. Untuk sebagian besar tujuan, molaritas adalah unit konsentrasi yang disukai. Jika suhu percobaan akan berubah, maka satuan yang baik untuk digunakan adalah molalitas . Normalitas cenderung paling sering digunakan untuk perhitungan titrasi.

Kimia 12 Molaritas Molalitas dan Fraksi Mol YouTube
KOMPAS.com - Larutan memiliki beberapa jenis sifat koligatif, salah satunya adalah molalitas.Apa yang dimaksud dengan molelitas dan bagaiamana rumus molalitas?Berikut adalah penjelasannya! Pengertian molalitas. Dilansir dari Chemistry LibreTexts, molalitas adalah cara menyatakan konsentrasi larutan. Molalitas merupakan jumlah mol suatu zat terlarut dalam satu kilogram atau 1.000 gram pelarut.