
Hukum Kelipatan Perbandingan Dalton Kimia Kelas 10 YouTube
Hukum Perbandingan Berganda (Hukum Dalton) berbunyi: "Jika dua jenis unsur bergabung membentuk lebih dari satu senyawa, dan massa salah satu unsur dalam senyawa itu sama, sedangkan massa unsur lain berbeda, maka perbandingan massa unsur lainnya dalam senyawa tersebut merupakan bilangan bulat dan sederhana." Baca juga:

Hukum Dalton Bunyi dan Contoh Soal
Hukum Dalton tentang tekanan parsial digunakan untuk menentukan tekanan individu masing-masing gas dalam campuran gas. Hukum Dalton tentang Tekanan Parsial Tekanan total campuran gas sama dengan jumlah tekanan parsial gas komponen. Tekanan Total = Tekanan Gas 1 + Tekanan Gas 2 + Tekanan Gas 3 +. Tekanan Gas n

PPT Hukumhukum tentang Gas PowerPoint Presentation, free download ID5902339
5 Hukum Dasar Kimia. 1. Hukum Lavoisier (Hukum Kekekalan Massa) 2. Hukum Proust (Perbandingan Tetap) 3. Hukum Dalton (Kelipatan Perbandingan) 4. Hukum Gay Lussac (Perbandingan Volume) 5. Hipotesis Avogadro. Jakarta -. Berbicara tentang ilmu kimia tampaknya tak bisa lepas dari hukum dasar kimia yang sudah menjadi aturan sejak abad ke-18.

Percobaan teori hukum Dalton dan Gay Lussac kelompok 1 YouTube
1. Hukum Lavoisier 2. Hukum Proust (Hukum Perbandingan Tetap) 3. Hukum Dalton (Hukum Perbandingan Berganda) 4. Hukum Gay Lussac (Hukum Perbandingan Volume) 5. Hipotesis Avogadro Contoh Soal 1 (Hukum Lavoisier) Contoh Soal 2 (Hukum Proust) Contoh Soal 3 (Hukum Dalton) Contoh Soal 4 (Hukum Gay Lussac)

Hukum Dalton Bunyi Dan Contoh Soal SoalB
Hukum Dalton tentang Tekanan Parsial, atau Hukum Dalton, menyatakan bahwa tekanan total gas dalam wadah adalah jumlah dari tekanan parsial masing-masing gas dalam wadah.. Definisi Tekanan dan Contohnya. Hukum Kimia. Nama dan Kegunaan 10 Gas Umum. Hukum Kimia. Komposisi Kimia Udara. Kimia. Kamus Kimia A sampai Z. Proyek & Eksperimen.

Suatu contoh hukum perbandingan berganda Dalton yaitu pem...
Hukum Dalton disebut juga sebagai Hukum Perbandingan Berganda. John Dalton menyatakan bahwa materi terdiri atas atom yang tidak dapat dibagi lagi. Tiap-tiap unsur terdiri atas atom-atom dengan sifat dan masa identik, dan senayawa terbentuk jika atom dari berbagai unsur bergabung dalam dalam komponen yang tetap.

Hukum Dalton
Hukum Dalton Pengertian hukum perbandingan berganda apabila dua buah unsur bersenyawa, jenis persenyawaan yang terbentuk dapat berupa lebih dari satu. Misalnya sebagai contoh hukum perbandingan berganda dalton yaitu ketika hidrogen dan oksigen bergabung dapat terbentuk air ( H2O) atau hidrogen peroksida ( H2O2 ).

Hukum Kelipatan Perbandingan (Dalton) Materi Hukum Dasar Kimia Kimia SMA Pojan.id YouTube
Hukum Dalton merupakan salah satu dari cabang ilmu kimia, ilmu yang mempelajari tentang unsur yang terdapat pada makhluk hidup dan tidak hidup. Hukum yang melengkapi bagian dari teori sebelumnya, hukum perbandingan tetap dari Proust dan hukum kekekalan massa dari Lavoiser.

Hukum Dalton Isi Penerapan Rumus dan Contoh Soal
Hukum Dalton menyatakan bahwa campuran gas terdiri dari berbagai macam gas yang masing-masing bisa dihitung volumenya secara terpisah. Konsep ini sangat berguna dalam dunia pendidikan, terutama di bidang ilmu kimia. Mari kita cari tahu lebih lanjut tentang konsep Hukum Dalton dan contohnya dalam pendidikan dalam artikel ini.

Hukum Dalton beserta Contoh dan Latihan soal
ISI HUKUM DALTON 1. Bunyi Hukum Dalton 2. Definisi Atom 3. Struktur Atom 4. Pembentukan Senyawa 5. Reaksi Kimia 6. Pembatasan Hukum Dalton 7. Prinsip Perhitungan Hukum Dalton 1. Perbandingan internal 2. Perbandingan eksternal 8. Contoh Penerapan Hukum Dalton Lain Dalam Hitungan 1. Karbon dan Oksigen 2. Sulfur dan Oksigen 3. Hidrogen dan Oksigen

HUKUM DALTON DAN GAY LUSSAC YouTube
TRIBUNNEWS.COM - Pengertian hukum perbandingan berganda atau hukum Dalton. Hukum Dalton pertama kali didukung dan dikemukakan oleh John Dalton yang merupakan ahli kimia. John Dalton.

Hukum Kelipatan Perbandingan Dalton
Contoh Soal Hukum Dalton. 1. Unsur nitrogen dan oksigen dapat membentuk lebih dari satu senyawa,misalnya NO, NO2, N2O2 dan N2O4. Pada kondisi tertentu, 1 gram nitrogen tepat bereaksi dengan 1,14 gram oksigen. Pada kondisi yang lain, 1 gram nitrogen tepat bereaksi dengan 2,28 gram oksigen. Jelaskan bahwa data ini sesuai dengan Hukum Perbandingan.

Hukum Perbandingan Berganda Milik Dalton, Ini Pengertiannya!
Sonora.ID - Hukum Dalton merupakan salah satu hukum dasar kimia yang diciptakan oleh seorang seorang ahli fisika sekaligus meteorologis asal Inggris yang bernama John Dalton pada tahun 1803. Mulanya, Dalton sedang meneliti perihal berat atomik, lalu dia tiba-tiba mendapatkan ide untuk meneliti tentang senyawa.
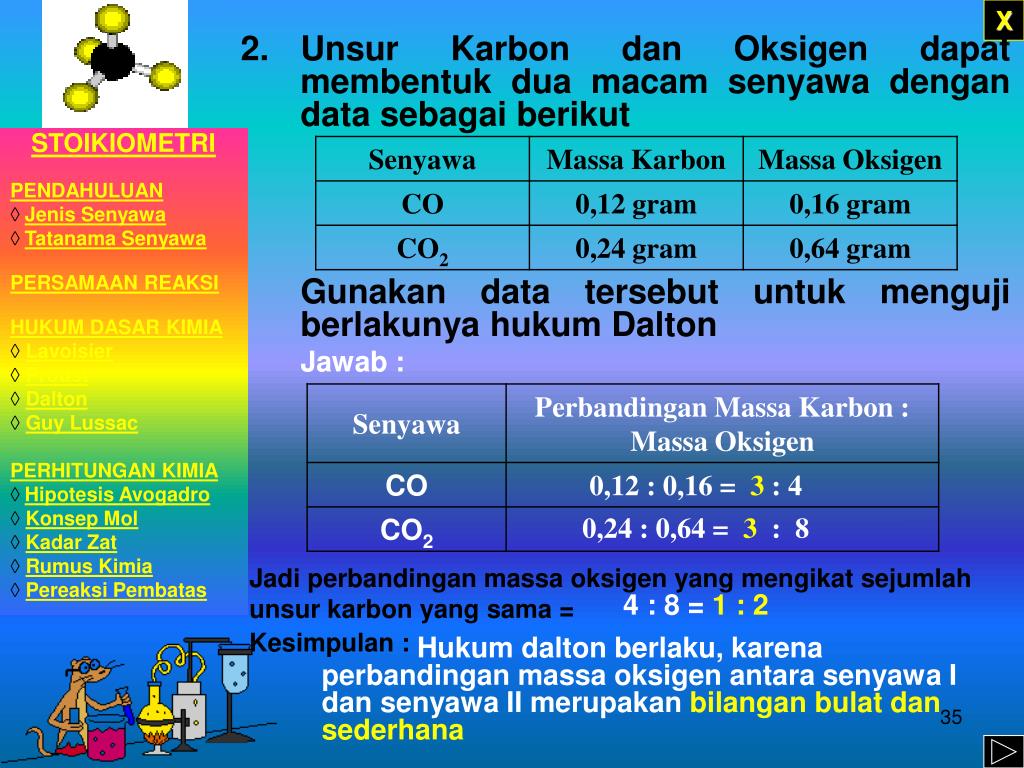
Perbandingan Massa Unsur Oksigen Dalam Dua Senyawa Tersebut Sesuai Hukum Dalton Adalah
Hukum Dalton adalah hukum yang menyatakan apabila unsur-unsur dapat membentuk beberapa senyawa dan massa salah satu unsur selalu tetap, perbandingan massa unsur yang lain dapat dinyatakan dalam bilangan bulat dan sederhana.

Hukum Dalton PDF
Apakah hukum Dalton berlaku untuk senyawa tersebut. Pembahasan Untuk menjawab soal ini kita buat tabel hasil reaksi antara belerang dengan nitrogen seperti dibawah ini. Dengan perbandingan massa belerang sama (1 : 1) maka kita peroleh perbandingan massa oksigen senyawa I dan II yaitu sebagai berikut: Massa Oksigen I Massa Oksigen II = 1 1,5 = 2 3

Contoh Soal Hukum Dasar Kimia Dalton
Hukum Perbandingan Berganda (Hukum Dalton , 1766 - 1844) Dalton menyelidiki bahwa perbandingan massa unsur - unsur pada setiap senyawa dan mendapatkan sebuah pola keteraturan. Pola tersebut dinyatakan sebagai hukum perbandingan berganda yang menegaskan bahwa kedua unsur yang dapat membentuk 2 senyawa atau lebih memiliki perbandingan.