
Sifat Koligatif Larutan Perbedaan Molaritas Dan Molalitas Halaman All Riset
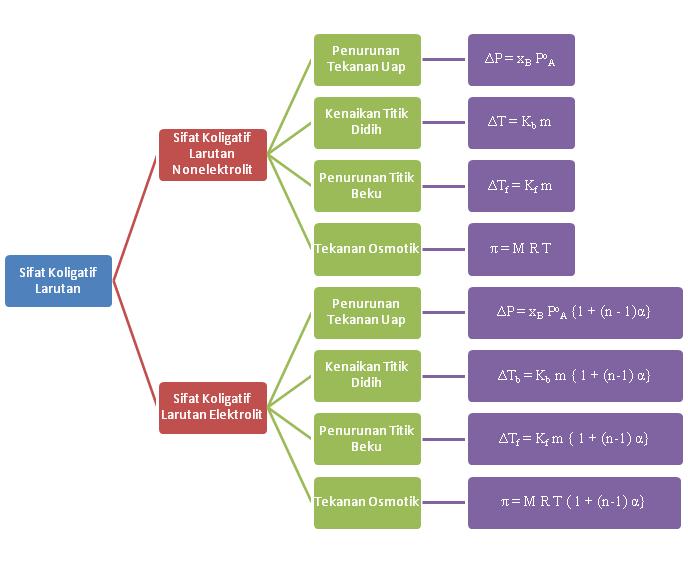
Jumlah partikel larutan elektrolit lebih banyak daripada larutan non-elektrolit sehingga sifat koligatifnya pun akan lebih besar. Nilai dari sifat koligatif larutan non-elektrolit dapat diketahui dengan rumus-rumus berikut ini: Penurunan tekanan uap. ΔP = P⁰.
Mengenal Pengertian Larutan Elektrolit Dan Non Elektrolit Sifat Ciri Unamed
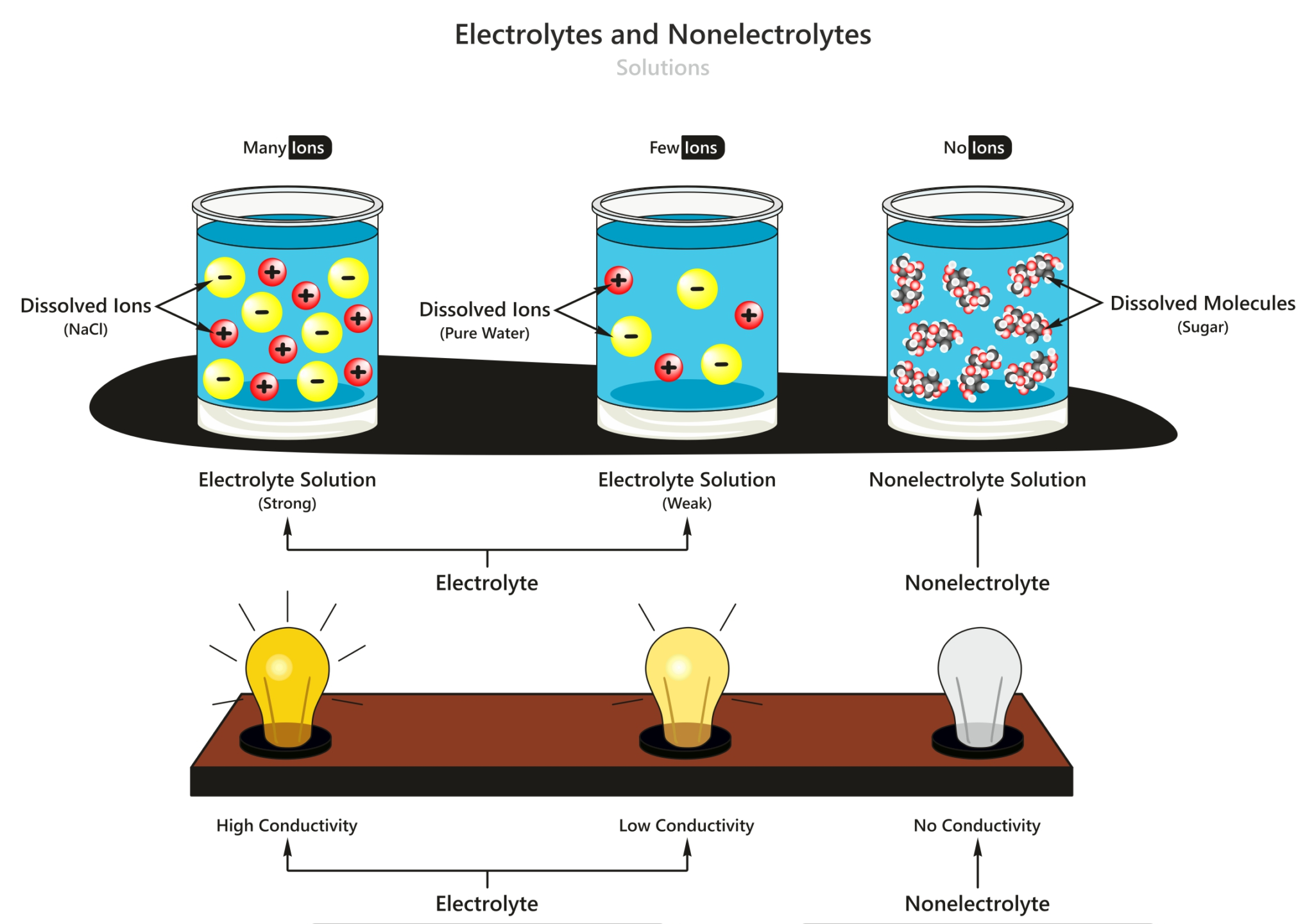
Terlepas dari konsep larutan yang dapat beredar melalui beberapa media (air, gas, dan benda padat), klasifikasi larutan elektrolit dan non elektrolit didasarkan pada sifat daya hantar listriknya. Oleh karena itu, bahasan larutan elektrolit dan non elektrolit bukan berfokus pada pelarut, tetapi zat yang terlarut di dalamnya.
Sifat Koligatif Larutan Elektrolit dan Larutan Non Elektrolit Materi Kimia
Larutan non elektrolit gula (sukrosa) 0,01M → ∆ Tf =0,186 o C. Larutan NaCl yang konsentrasinya 0.01M → ∆ Tf =0,348 o C. Secara umum dapat disimpulkan bahwa, Untuk konsentrasi yang sama, larutan elektrolit mempunyai sifat koligatif larutan yang lebih besar dibandingkan larutan non elektrolit. Kemolalan dan Fraksi Mol Molalitas (m)

Larutan Elektrolit dan Non Elektronik Beserta Contoh Elektrolit Belajar IPA
Berikut adalah manfaat larutan non elektrolit. 1. Sebagai sumber energi. Gula adalah salah satu komponen larutan non elektrolit. Gula ini merupakan sumber energi dalam bentuk karbohidrat sederhana. Ketika tubuh manusia kekurangan gula, maka akan terasa lelah, jantung berdebar, dan sulit berkonsentrasi.

PPT ** Tugas bahan ajar Kimia** PowerPoint Presentation, free download ID5411227
Larutan elektrolit tinggi memiliki derajat ionisasi (α) yang mendekati 1, berarti zat terlarut hampi semuanya terionisasi. Adapun larutan elektrolit lemah memiliki derajat ionisasi jauh dibawah 1, berarti zat terlarut yang berubah menjadi ion hanya sedikit. Hal ini menyebabkan larutan elektrolit lemah menghantarkan listrik dengan kurang baik.

PPT LARUTAN ELEKTROLIT DAN NON ELEKTROLIT PowerPoint Presentation, free download ID4715206
Sifat koligatif larutan merupakan sifat larutan yang bergantung pada banyaknya zat terlarut dan tidak tergantung pada jenis zat terlarut. Sifat koligatif larutan dibagi menjadi dua jenis, yaitu: sifat koligatif larutan elektrolit dan larutan non elektrolit. Sifat Koligatif Larutan Elektrolit 1. Kenaikan titik didih ∆Tb = Kb . m { 1 + (n-1) α} Keterangan: ∆Tb =

Larutan Elektrolit dan Non Elektrolit (Kompone
Sedangkan sifat koligatif dari larutan nonelektrolit memiliki nilai yang lebih rendah dikarenakan tidak terjadi disosiasi pada larutan nonelektrolit. Jadi, perbedaan sifat koligatif larutan elektrolit dan non elektrolit adalah pada nilai disosiasinya yang dapat mempengaruhi besar kecilnya sifat koligatif.

Contoh Larutan Elektrolit Kuat Lemah Beserta Perbedannya Riset
Pada larutan non-elektrolit faktor van't Hoff nya bernilai 1 karena tidak memiliki ion, sehingga tidak diperlukan faktor van't Hoff dalam perhitungan sifat koligatifnya. Sifat koligatif pada larutan elektrolit sama dengan sifat koligatif non-elektrolit yaitu penurunan tekanan uap jenuh, kenaikan titik didih, penurunan titik beku, dan.

Contoh Larutan Elektrolit Kuat Dan Lemah Berbagai Contoh
Sifat koligatif sendiri hanya memandang "kuantitas", bukan "kualitas". Oleh sebab itu, sifat larutan, seperti rasa, warna, dan kekentalan (viskositas) merupakan sifat-sifat yang bergantung pada jenis zat terlarut yang tercampur dalam larutan. Terdapat empat sifat koligatif larutan, yaitu penurunan tekanan upa, kenaikan titik didih.

SifatSifat Larutan Elektrolit dan Nonelektrolit Memotivasi Diri
Pada umumnya semua senyawa ionik yang mudah larut dalam air, seperti NaCl, KBr, CuCl 2, Ca(NO 3) 2, (NH 4) 2 S, dan NaOH adalah elektrolit kuat. Namun, untuk senyawa ionik yang cenderung sukar larut dalam air seperti CaC 2 O 4, SrCO 3, BaSO 4 dan AgCl, daya hantarannya akan cenderung lebih lemah.. 2.

Larutan Elektrolit dan Non Elektrolit (Kimia SBMPTN, UN, SMA) YouTube
Larutan Elektrolit dan Nonelektrolit - Kata elektrolit berasal dari bahasa Yunani Kuno, yakni ήλεκτρο- (ēlectro-), sebuah awalan yang berkaitan dengan listrik, dan λυτός (lytos) yang berarti "dapat dilepaskan atau dilonggarkan".Secara definisi, larutan elektrolit merupakan larutan yang dapat menghantarkan listrik sedangkan larutan non-elektrolit merupakan larutan yang tidak.

Mengenal Larutan Elektrolit dan Non Elektrolit Kimia Kelas 10
Sifat koligatif larutan adalah sebuah karakter yang dimiliki di dalam sebuah larutan. Karakter zat itu sangat tak tergantung pada komponen terlarut lain dan jenis zat larutan bersangkutan. Pada dasarnya, sifat koligatif pada suatu larutan mempunyai 2 macam yakni sifat koligatif non elektrolit dan sifat koligatif elektrolit.
Memahami Larutan Elektrolit dan Nonelektrolit beserta Contohnya Kimia Kelas 10 Belajar
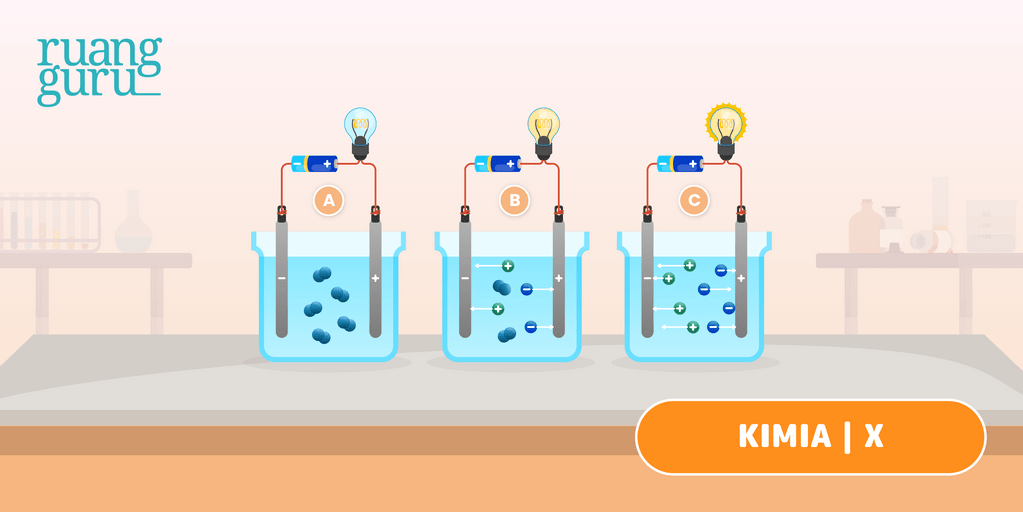
Larutan elektrolit yang memberikan gejala berupa lampu menyala dan membentuk gelembung gas disebut elektrolit kuat. Contohnya yaitu HCl, air aki, air laut, dan air kapur. Adapun elektrolit yang tidak memberikan gejala lampu menyala tetapi menimbulkan gelembung gas termasuk elektrolit lemah. Contohnya yaitu larutan amonia, larutan cuka,dan.

Larutan Elektrolit dan Nonelektrolit
Sifat Koligatif Larutan Non-Elektrolit. Di tengah pandemi Covid-19, Tim Pengabdian Masyarakat Departemen Kimia Kedokteran, Fakultas Kedokteran Universitas Indonesia (FK UI) tengah membuat produk hand sanitizer dalam jumlah banyak untuk dibagikan kepada rumah sakit hingga sekolah. (Dok.

30 Contoh Larutan Elektrolit dan Non Elektrolit
Van't Hoff menyatakan bahwa pada konsentrasi yang sama, larutan elektrolit akan memiliki sifat koligatif yang lebih besar daripada larutan non elektrolit. Hal tersebut dikarenakan pada larutan elektrolit jumlah partikelnya lebih banyak daripada larutan non elektroit sesuai pembahasan sebelumnya mengenai perbedaan larutan elektrolit dan non.

Larutan Elektrolit dan Non Elektrolit (Komponen Larutan)
Sifat koligatif larutan terbagi menjadi dua, yaitu: sifat koligatif larutan elektrolit dan sifat koligatif larutan non elektrolit. Perbedaan antara sifat koligatif larutan elektrolit dan non elektrolit adalah sebagai berikut: Sifat Koligatif Larutan Elektrolit Dapat mengalami ionisasi (terurai menjadi ion-ion penyusunnya) Dipengaruhi faktor Van't Hoff (i), sehingga sifat koligatif larutan.