
Lihatlah Gambar Berikut Gambar Yang Menunjukkan Aliran Elektron Adalah serat
Perpindahan elektron dari satu benda (yang kemudain menjadi bermuatan positif) ke benda lain (yang kemudian menjadi bermuatan negatif). Pembahasan: Listrik statis adalah fenomena kelistrikan dimana muatan listriknya tidak bergerak. Suatu benda dapat dibuat bermuatan listrik statis baik negatif atau positif, akibat sentuhan, gesekan atau kontak.

Diagram orbital dan Konfigurasi elektron kimia SMA YouTube
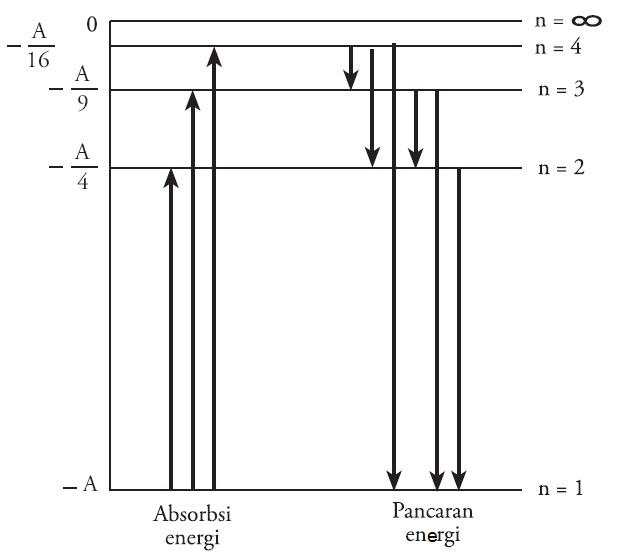
Jika elektron kembali ke tingkat energi yang lebih rendah, akan disertai pelepasan energi berupa gelombang elektromagnet (pemancaran radiasi). Bentuk energi yang dilepaskan ke lingkungan dapat berupa emisi cahaya ultraviolet (UV), emisi cahaya tampak (visible), atau emisi panas (infra red). Energi radiasi yang dipancarkan sama dengan selisih.

Dalam waktu satu jam terjadi perpindahan elektron sebanya...
Jadi, sebenernya, perpindahan elektron itu bisa terjadi dari tubuh kita ke benda, maupun sebaliknya, ya. Nah, untuk kasus ini, memang umumnya perpindahan elektronnya itu dari tangan ke gagang pintu. Kenapa nggak sebaliknya? Kalo dari gagang pintu ke tangan itu cukup sulit terjadi, karena si gagang pintunya perlu untuk digosok-gosok terlebih.

Konsep Perpindahan Elektron Kelas 9 SMP YouTube
Perpindahan itu tak memunculkan masalah walaupun jarak perpindahan kelereng pendek. Jadi, dari contoh itu dapat dikatakan bahwa dalam bidang listrik, pengaruh dari bahan konduktor yang satu ke konduktor lainnya memiliki kecepatan yang sama dengan kecepatan cahaya atau kurang lebih 186.000 mil per detik. 2. Aliran Elektron dari Sumber ke Tujuan

PPT METABOLISME ENERGI PowerPoint Presentation, free download ID6083905
Pengetahuan dasar tentang teori kelistrikan. Membicarakan tentang kelistrikan pada dasarnya adalah membicarakan segala sesuatu yang menyangkut perpindahan elektron karena adanya impuls yang menyebabkannya. Pola berpindahnya elektron-elektron sehingga menimbulkan energi listrik serta upaya pengaplikasiannya di dalam berbagai penerapan adalah.

Gambar Berikut Yang Menunjukkan Aliran Elektron Adalah Lengkap
Perpindahan tersebut akan menyebabkan penyerapan energi ketika suatu elektron berpindah dari lintasan rendah ke tinggi. Oke, sampai sini paham ya. Singkatnya, atom Bohr punya 3 postulat atau bisa kita sebut juga dengan gagasan utama dalam teori atom Niels Bohr sebagai berikut: Elektron mengitari inti bermuatan positif dalam lintasan lingkaran.
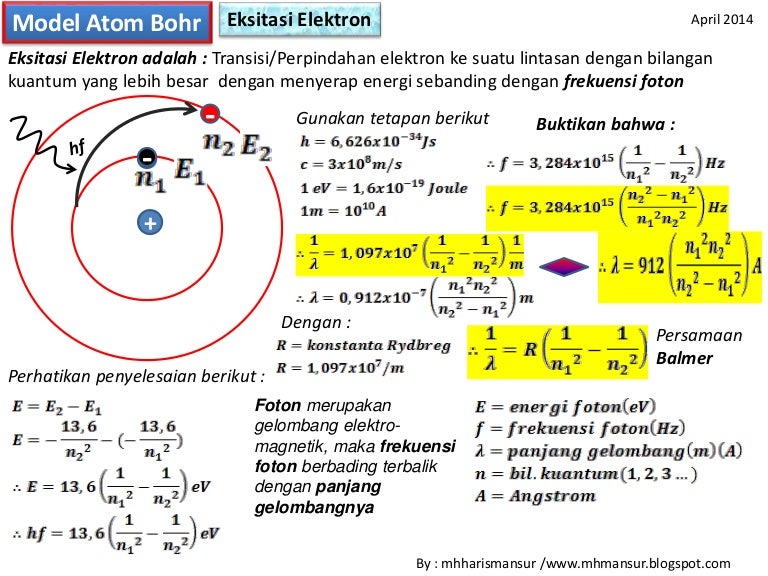
Model atom bohr(eksitasi elektron)
Elektron yang mengelilingi atom bisa pindah dari satu lintasan ke jalur lain; Jika elektron pindah ke lintasan yang lebih tinggi, ia akan melakukan penyerapan energi;. Sedangkan deeksitasi, dijelaskan sebagai perpindahan energi dari tingkat tinggi ke yang lebih rendah dari sebelumnya. Proses ini terjadi akibat adanya sebuah pemancaran energi.

Bioluminesensi dan Biofluoresensi
Perpindahan muatan ini terjadi karena adanya dua buah benda yang saling bergesekan. Sebagaimana debu yang terbang bersama udara bergesek dengan permukaan layar TV. Dari gesekan tersebutlah, terjadi perpindahan muatan elektron. Nah, ketika muatan elektron berpindah, kedua benda bisa mengalami kelebihan elektron sehingga bermuatan negatif.
Video belajar Perpindahan Elektron IPA untuk Kelas 9
Bukan petirnya Thor yaa, tapi petir yang sering kita lihat. Petir bisa terjadi karena awan yang bergesekan satu sama lain. Setelah proses pergesekan, terbentuklah elektron-elektron bebas yang kemudian saling berkumpul, sehingga memiliki cukup beda potensial untuk menyambar permukaan bumi. Saking berbahayanya petir, kini dibuat alat penangkal.

Tabel Perpindahan Elektron Yang Benar Listrik Statis & Dinamis UCUN IPA SMP 2019 no 15 YouTube
Perpindahan muatan ini terjadi karena adanya dua buah benda yang saling bergesekan. Sebagaimana debu yang terbang bersama udara bergesek dengan permukaan layar TV. Dari gesekan tersebutlah, terjadi perpindahan muatan elektron. Nah, ketika muatan elektron berpindah, kedua benda bisa mengalami kelebihan elektron sehingga bermuatan negatif.
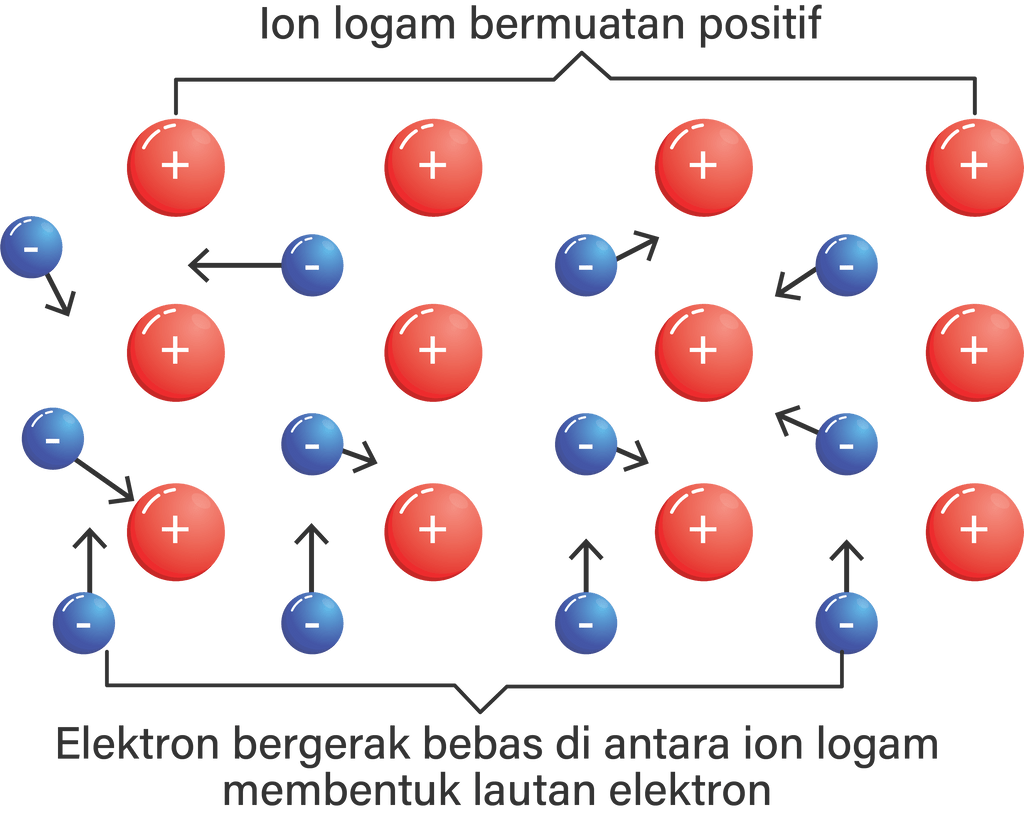
Kedudukan elektronelektron dari atomatom logam d...
Efek listrik statis dapat terjadi karena adanya perpindahan elektron. Benda menjadi bermuatan karena muatan negatifnya (elektron) dipindahkan dari satu benda ke benda lain. Jadi menggosok penggaris dengan kain artinya kedua benda saling dimuati (charged) sehingga elektron dari salah satu benda berpindah ke benda lain..
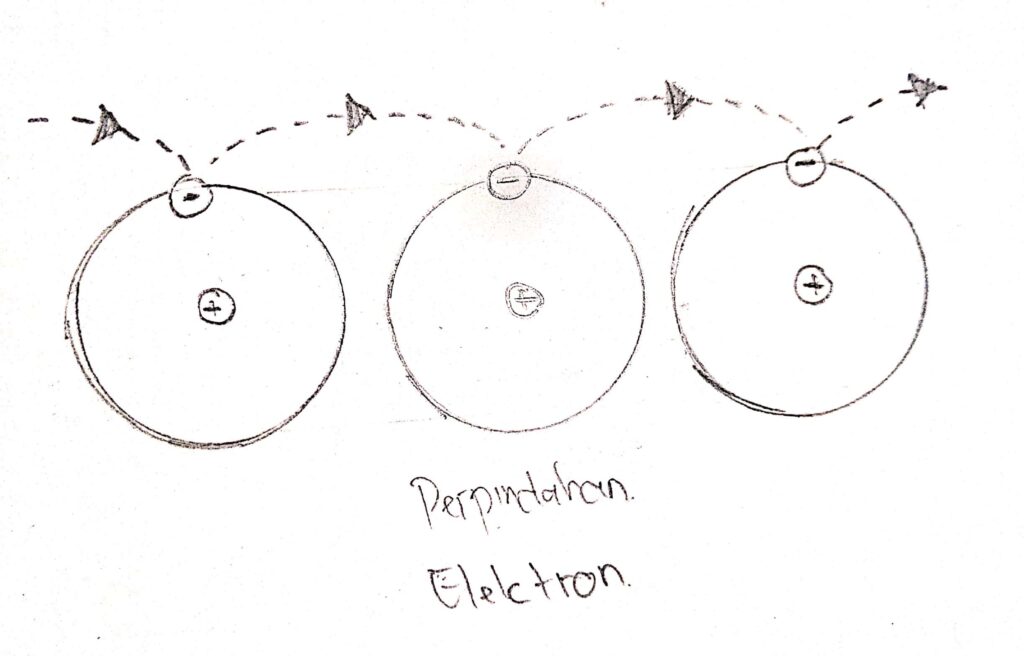
Partikel Atom dalam Kelistrikan Si Paling Elektro
Perpindahan elektron tersebut terjadi secara terus-menerus hingga menghasilkan arus listrik. Baca juga: Pengertian dan Prinsip Kerja Sel Volta. Jenis-jenis sel elektrokimia. Secara garis besar, sel elektrokimia terbagi menjadi dua yaitu sel galvani atau sel volta dan juga sel elektrolisis.

Apa yang terjadi apabila benda A.dan B.memiliki elektron
Dilansir dari Circuit Globe, energi listrik adalah energi yang ditimbulkan oleh perpindahan elektron dari suatu tempat ke tempat lain. Aliran elektron berpindah karena adanya beda potensial di satu tempat dengan tempat lainnya. Adapun, elektron adalah muatan listrik negatif. Karena energi listrik terbentuk dari pergerakan muatan listrik, maka.
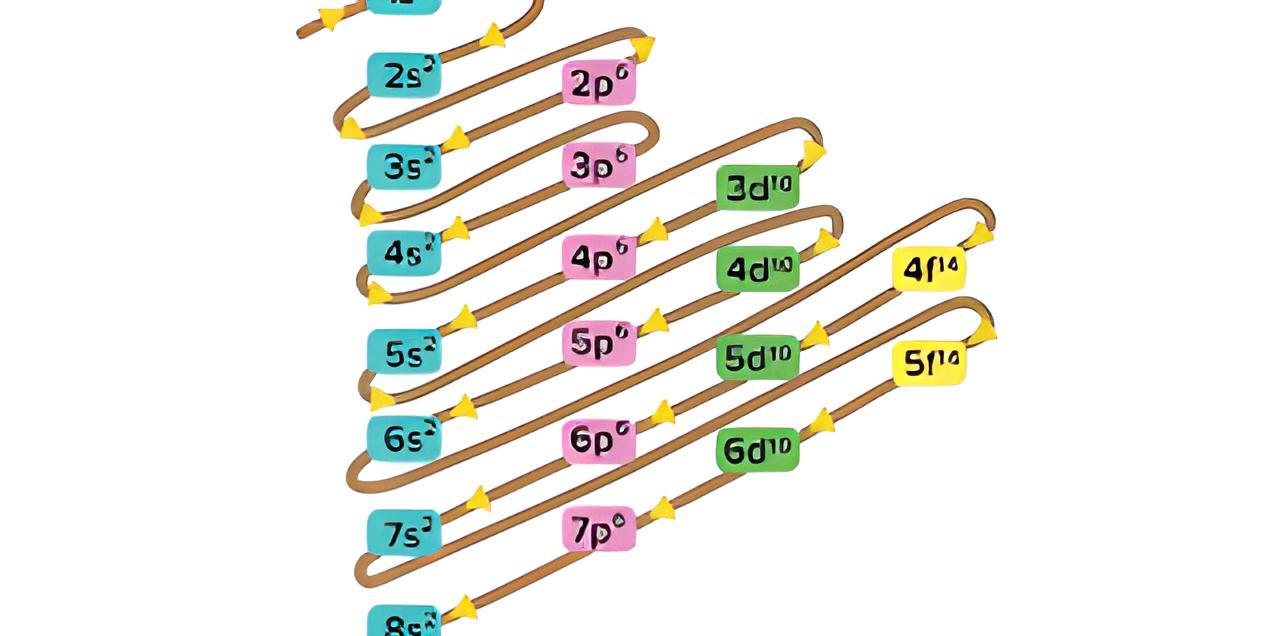
Aturan Konfigurasi Elektron Dan Diagram Orbital Superprof
Bilangan kuantum spin ini dilambangkan dengan s. Setiap kali orbit memuat 2 elektron dengan arah rotasi yang berlawanan, maka: Searah putaran jarum jam atau ke arah atas dengan notasi +1/2. Berlawanan arah jarum jam atau ke arah bawah dengan notasi -1/2. B. Transisi Elektron. Transisi elektron merupakan perpindahan 1 orbit ke orbit lainnya.
Teori Atom Mekanika Kuantum Werner Heisenberg, Erwin Schrodinger
Konsep Reaksi Redoks berdasarkan Perpindahan Elektron. Berdasarkan perpindahan (transfer) elektron, reaksi reduksi adalah reaksi penangkapan elektron, sedangkan reaksi oksidasi adalah reaksi pelepasan elektron. Bisa kamu perhatikan gambar di atas ya, pada reaksi reduksi, elektronnya berada di ruas sebelah kiri reaksi, sebagai reaktan.

Cara Menentukan Arah Arus Listrik Maupun Arus Elektron Listrik Dinamis IPA Kelas 9 YouTube
Pada baterai biasa (baterai karbon-seng), yang menjadi katoda adalah seng, yang juga menjadi pembungkus baterai. Sedangkan, pada baterai alkalin, yang menjadi katoda adalah mangan dioksida (MnO2) (Riyanto, 2012). Reaksi elektrokimia melibatkan perpindahan elektron-elektron bebas dari suatu logam kepada komponen di dalam larutan.