
Ikatan ion I rumus molekul senyawa ion I energi kisi I siklus Born Haber I Sifat sifat senyawa
Perbandingan beberapa sifat senyawa kovalen dan ion : Tabel 1. perbandingan sifat senyawa kovalen dan senyawa ion. No Senyawa kovalen Senyawa ion 1 Kebanyakan menunjukkan titik Kebanyakan menunjukkan titik leleh rendah (<350oC). leleh tinggi (>350oC, sering sampai 1000oC). 2 Umumnya cairan atau gas pada Semuanya dalah padatan pada suhu kamar.

Konsep Mudah Belajar Rumus Senyawa dan Nama Senyawa Ion KIMIA SMA YouTube
Sifat fisis senyawa ion antara lain titik leleh dan titik didih yang tinggi, larut dalam pelarut air, bersifat konduktor listrik. Pada saat atom-atom membentuk ikatan, hanya elektron-elektron pada kulit terluar yang berperan yaitu elektron valensi. Elektron valensi dapat digambarkan dengan struktur Lewis yaitu lambang kimia suatu atom atau ion.

Sebutkan Sifat Sifat Senyawa Ion
Beberapa sifat senyawa ion antara lain: 1. Kristalnya keras tetapi rapuh. Apabila senyawa ion dipukul, akan terjadi pergeseran posisi ion positif dan negatif, dari yang semula berselang-seling menjadi berhadapan langsung. Hal ini menyebabkan ion positif bertemu muka dengan ion positif dan terjadi gaya tolak-menolak.

SifatSifat Senyawa Ion Apa yang Perlu Diketahui? PT ICSA
Semua yang ada di dunia ini memiliki sifat-sifatnya masing-masing. Begitu juga dengan senyawa ion dan kovalen. Mereka juga memiliki sifatnya sendiri sehingga bisa menjadi pembeda dengan senyawa yang lain. Sifat senyawa ion maupun sifat senyawa kovalen dapat kita jabarkan sebagai berikut. 1. Sifat-sifat senyawa ion Titik didih dan titik leleh tinggi Mudah larut dalam pelarut

Pengertian,Sifat Dan Contoh Dari Senyawa Ion KIMIA OKE PINTAR
Sifat-sifat senyawa ion sangat menarik dan penting dalam kimia. Mari kita sebut dan jelaskan sifat-sifat ini secara runtut dan detail: 1. Titik Lebur dan Titik Didih Tinggi. Senyawa ion biasanya memiliki titik lebur serta titik didih tinggi. Hal ini disebabkan oleh gaya tarik elektrostatis kuat antara ion-ion dengan muatan berlawanan di dalam.
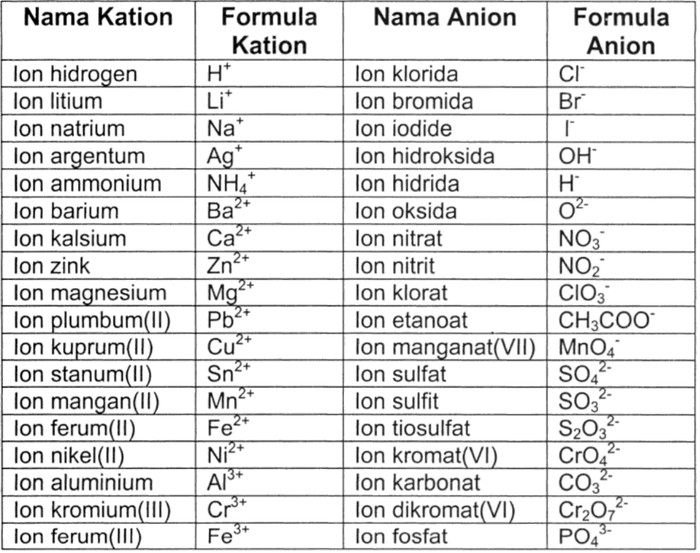
4 Sifat Senyawa Ion dan Contohnya
2.2 Sifat Senyawa Ion Sifat-sifat senyawa ion antara lain adalah kebanyakan menunjukkan titik leleh tinggi, pada umumnya senyawa ion larut dalam pelarut polar (seperti air dan amoniak). Senyawa ion berwujud padat tidak menghantarkan listrik, karena ion positif dan negatifterikat kuat satu sama lain. Akan tetapi cairan senyawa ion akan.

Cara Belajar Kimia secara Cepat UNSUR TRANSISI
1. Sifat Fisik Senyawa Ion Senyawa ion adalah senyawa yang terbentuk dari dua atom yang saling berikatan karena adanya perpindahan elektron dari satu atom ke atom lain. Sifat fisik senyawa ion adalah sebagai berikut: Senyawa ion memiliki titik didih dan titik leleh yang tinggi Senyawa ion larut dalam pelarut polar Senyawa ion berwujud padatan berbentuk

MENULISKAN RUMUS KIMIA SENYAWA ION DARI KATION DAN ANION YouTube
4 Sifat Senyawa Ion. Untuk membedakan apakah suatu zat tergolong senyawa ion atau bukan, caranya adalah dengan memahami sifat-sifat yang dimiliki senyawa ion. Beberapa sifat-sifat dari senyawa ion antara lain: 1. Berbentuk padat dengan titik leleh dan titik didih relatif tinggi. 2.

Ikatan Ion Beserta Contoh Ikatannya Rumus Kimia
Ciri senyawa ionik yang pertama adalah terbentuk dari ikatan ion, yaitu jenis ikatan kimia yang terkuat. Dilansir dari Encyclopedia Britannica, ikatan ion terbentuk dari gaya elektristatik ketika elektron valensi dari suatu atom ditransfer secara permanen ke atom lain. Atom yang kehilangan elektron menjadi kation (bermuatan positif) dan yang.

Sifat Senyawa Ion Sinau
Berikut ini beberapa sifat fisis yang dipengaruhi oleh jenis ikatan yang dimiliki oleh suatu senyawa. 1. Titik Didih. Secara umum, senyawa ion mempunyai titik didih lebih tinggi dari kovalen. Titik didih berkaitan dengan gaya tarik-menarik antar partikel (kohesi). Jadi ada hubungan yang semakin kuat maka semakin tinggi titik didihnya.

CINTA KIMIA SENYAWA KOMPLEKS
Secara umum, senyawa memiliki 4 (empat) ciri-ciri utama, antara lain: - Terbentuk dari dua unsur atau lebih, yang disusun secara reaksi kimia biasa. - Memiliki perbandingan komposisi yang tetap. - Kehilangan sifat zat asalnya. - Bisa diuraikan secara kimia,tapi tidak secara fisika. Sifat-Sifat Senyawa.

Ciriciri dari senyawa ion dan senyawa kovalen
B. Sifat Senyawa Ion Sekarang kita akan membahas mengenai sifat atau karakteristik yang dimiliki oleh senyawa ion. Bicara mengenai sifat dari senyawa ion, kita pasti akan menjumpai bahwa sifat dari senyawa ion sangatlah berbeda dengan senyawa kovalen. mas dennis akan memaparkan sifat dari senyawa kovalen pada penjelasan dibawah ini : 1. Senyawa.
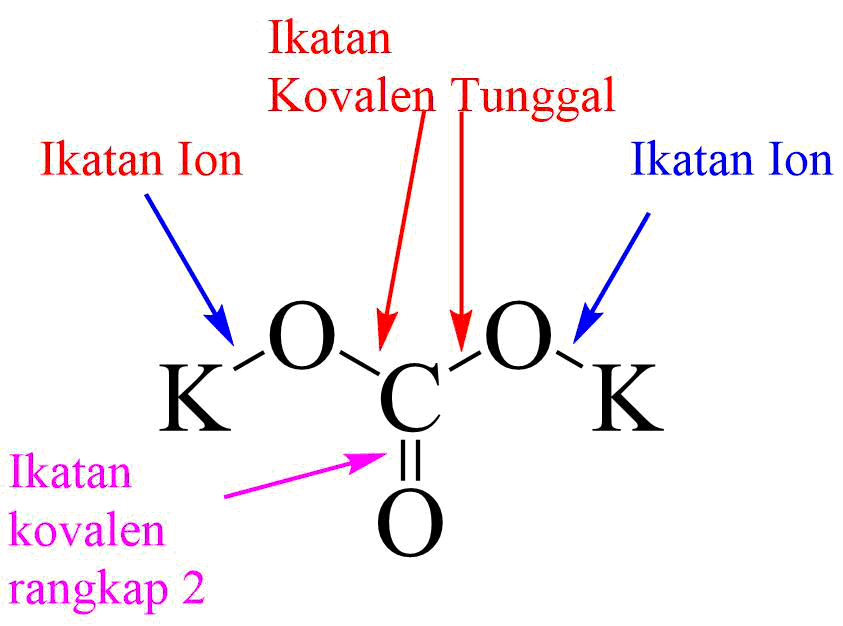
pengertian senyawa ion dan senyawa kovalen polar Matt Jackson
Oleh karena itu senyawa ion memiliki sifat-sifat sebagai berikut: 1. Senyawa ion yang padat tidak mudah menguap dan memunyai titik didih yang tinggi(600 sampai 200C) 2. Senyawa ion yang padat tidak menghantar listrik karena ion-ion yang bermuatan listrik itu telah terpaku kokok dalam posisi tertentu didalam ksis-kisi 3.

Ikatan Kimia Kelas 10 • Part 14 Sifat Senyawa Ion dan Kovalen, Ikatan Logam YouTube
Sebelum membahas sifat-sifat senyawa ion, kita perlu memahami terlebih dahulu apa itu senyawa ion. Senyawa ion merupakan senyawa yang terbentuk dari ion-ion positif dan negatif yang saling berikatan melalui interaksi elektrostatik. Ion positif disebut kation, sedangkan ion negatif disebut anion. Contoh senyawa ion yang umum dijumpai adalah NaCl.

Contoh Dari Senyawa Ion Dan Kovalen Garam dari unsur logam seperti licl , kcl ,mgcl2 , srbr2
Senyawa ionik adalah senyawa yang dibentuk dari ikatan ionik. Contohnya NaCl, KCl, BaCl2, dan BH4Cl. Sifat senyawa ionik antara lain: Senyawa ion mudah larut dalam air dan terdisosiasi menghasilkan ion-ion, sehingga larutannya bisa memiliki daya hantar listrik yang tinggi dalam keadaan terlarut dalam pelarut polar, dan rendah dalam keadaan padat.
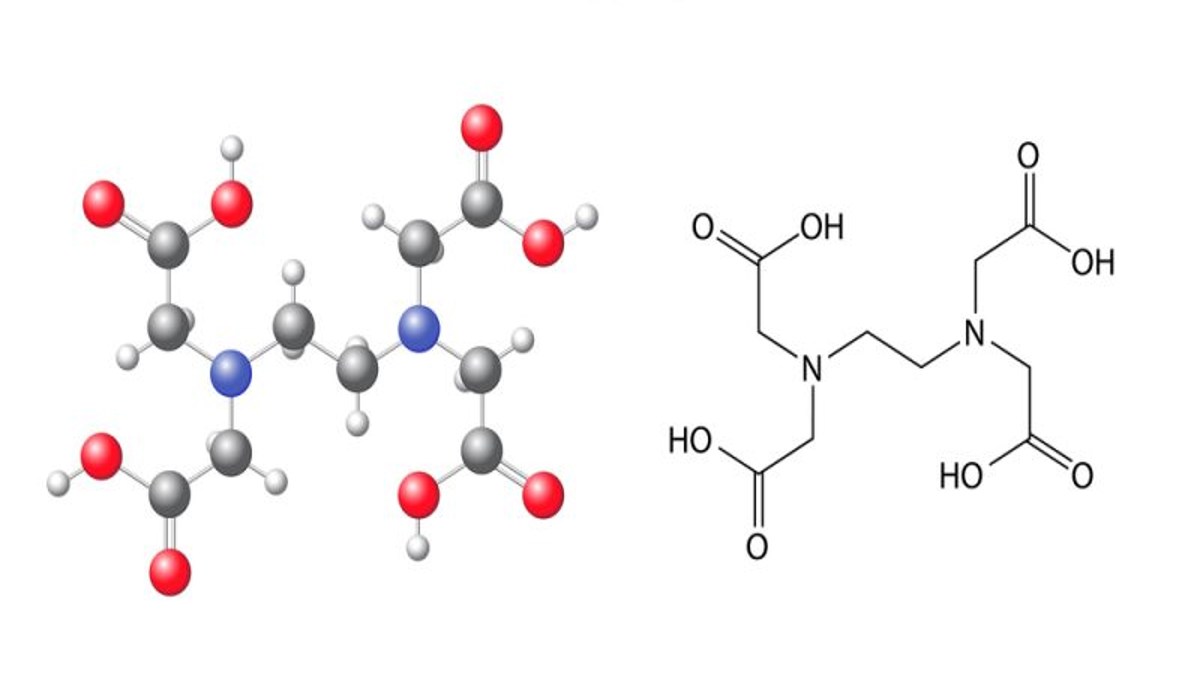
Sifat Senyawa Ion Bagian Atom yang Bermuatan Elektron, Ini Contohnya!
Beberapa sifat-sifat senyawa ion antara lain: 1. Titik leleh dan titik didih tinggi: Senyawa ion memiliki titik leleh dan titik didih yang lebih tinggi dibandingkan dengan senyawa kovalen. Hal ini disebabkan oleh gaya tarik elektrostatis yang kuat antara ion-ion yang saling berdekatan. 2. Konduktivitas listrik: Senyawa ion dapat menghantarkan.